印刷物の現物管理、回収管理ができます
お困りではありませんか?
いつ、だれが印刷したドキュメントかわからない
印刷したドキュメントの部数がかわからない
ドキュメントを回収したいが配布先がわからない
利用しなかったドキュメント管理が必要である
Di-Printerには解決策があります
ドキュメントに印刷証跡が印字されます
印刷した部数と何部目かがわかります
ドキュメントの配布先を管理できます
各ページにユニークなNOが振られ、ページ単位で管理できます
用途
誰が、いつ、どのプリンタで、何部、出力したかがわかるソリューションです。
監査証跡も取得していますので、データインテグリティも安心です。
利用方法
超簡単、印刷したいPDFをドラッグアンドドロップして、印刷するだけ
作業フロー
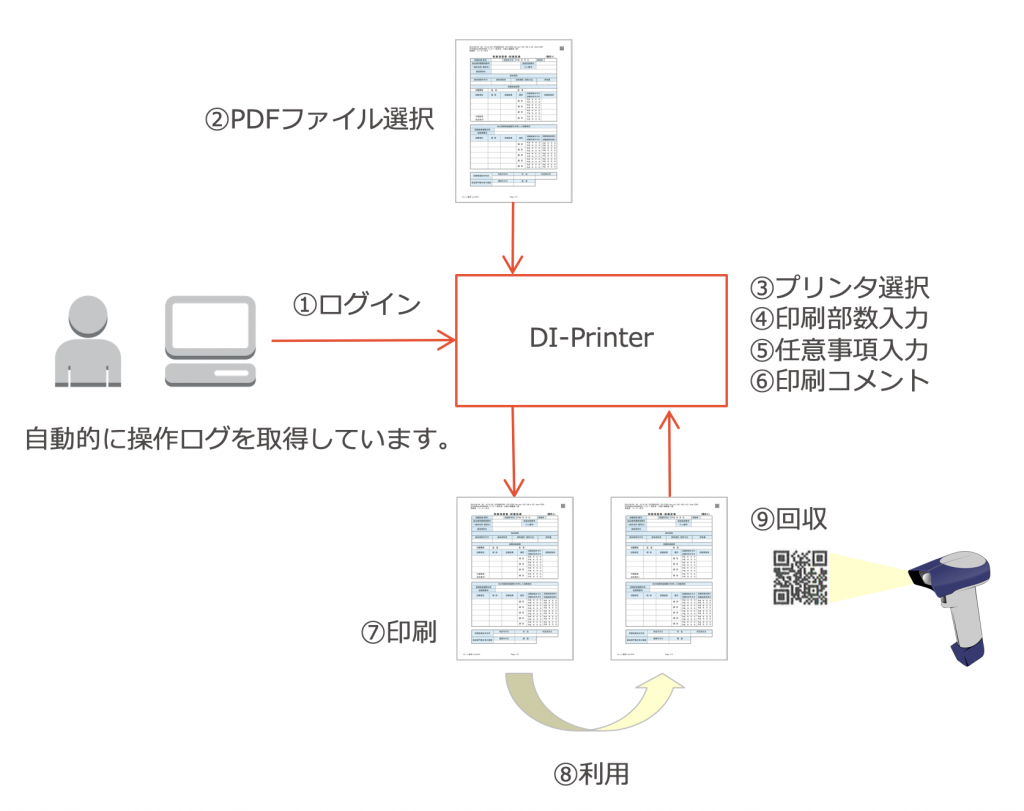
ログインして、PDFファイルをドラッグアンドドロップするだけ
PDFプリンターなどの論理プリンターには印刷できません
すべての用紙にユニークなバーコードが印刷されていますので、ページ毎の回収管理ができます
画面イメージ

入力項目
印刷者
配布部門
フリーエリア(右上、右下、左上、左下)
使用期限
印刷コメント
選択項目
プリンタ
両面・片面印刷
カラー・グレースケール
印刷イメージ

PDFイメージにヘッダーやフッターなどが追記されて、紙に印刷されます
標準機能
任意項目の登録
プリンタ選択
印刷
自動、任意項目の印刷
回収管理機能
監査証跡の閲覧
監査証跡のダウンロードなど
オプション機能
・印字項目・場所の変更
・CSV対応
・回収時期お知らせ機能
お客様のニーズに合わせてカスタマイズいたします。
自動印刷項目
・印刷日時(時分秒)|タイムスタンプ
時刻サーバより取得して利用 *1
・印刷プリンタ名称
・印刷者(本名アプリログイン者)
印刷の履歴になります。印刷者は本アプリの認証を経て印刷を実施していますので、なりすましなどは出来ません。
・印刷SEQNO|年度+月+SEQ8桁
・印刷SEQNO内のSEQ/総印刷部数
20180400000011
2018年04月の00000011番目の出力作業ということがわかります。
(3/5)総出力部数5の内の3番目の印刷物です。
・上記SEQNOのバーコード
配布した印刷物を回収する際にスキャンすると、その回収履歴が記録され、どれがあと何部戻ってきていないかがわかります。任意入力の配布先が入力されていれば、戻って来ていない配布先もわかります。
・ページ番号/総ページ番号
印刷部数1つのうちのページ番号を出力します。
*1 時刻サーバー
デフォルトでNICT公開NTPサービスを設定しています。日本標準時を提供する独立行政法人情報通信研究機構 (NICT) が運営をするPublic NTPサーバです。
また、設定画面で接続するサーバーを設定変更可能です。
任意印刷項目
・承認者氏名
任意項目の承認者を印刷します。
・配布先名|部数分
任意項目の配布部門を印刷します。印刷の部毎に印字内容が変わります。
・フリー項目|右上/右下/左上/左下
任意の項目を各ページの右上/右下/左上/左下に出力することが出来ます。
操作説明書
名称
Di-Printer v2.0
プログラムとマニュアル類
Di-Printer.exe Di-PRINTER本体プログラム
DiPrinter操作イメージ|20180806a.pdf
readme.txt
厚生労働省のコンピュータ化システムバリデーション(以下CSV)への対応は有償になります。弊社での設計、開発、テストドキュメントを御提供、貴社でのCSV作業のお手伝いをいたします。また、貴社ご要望に合わせたカスタマイズも承ります。
追加情報
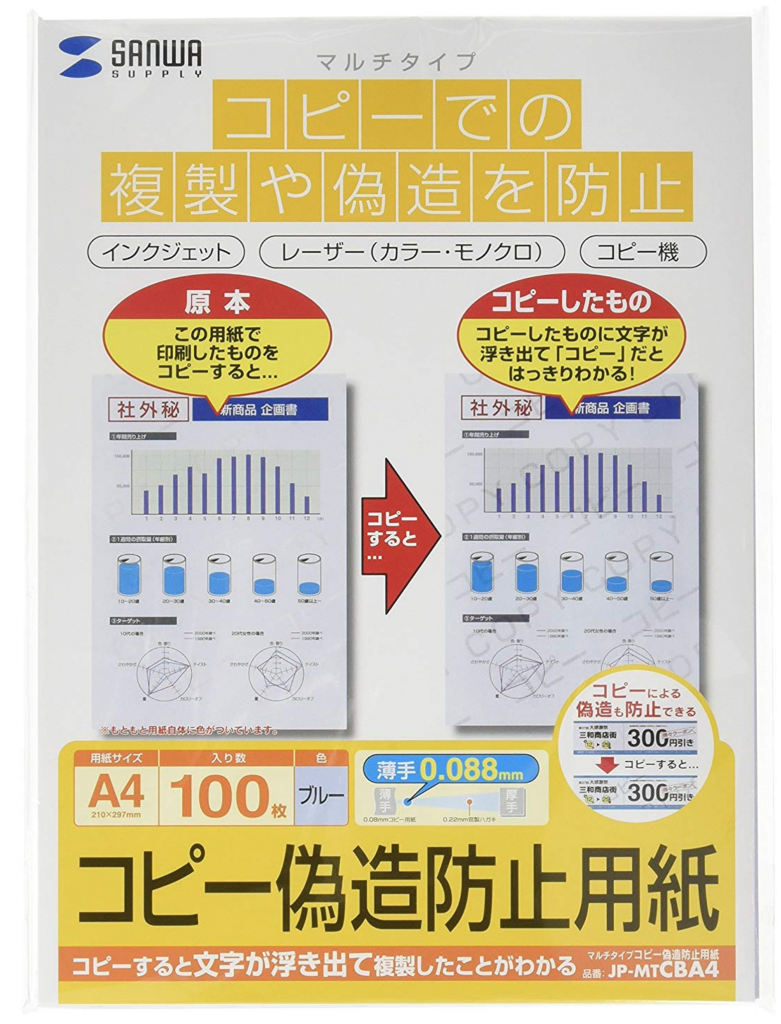
本ソフトウェアと左記のような”コピー偽造防止用紙”を合わせて利用いただければ、DI(Data Integrity)の要求を満たすことが可能となります
Amazonでご購入の場合は、こちらへ
DI(Data Integrity)関連製品

dbSheetClient
GxP CSV DI対応|EXCELソリューション
DIに対応して、EXCELが利用できます。詳細はこちら

Di-Printer
GxP CSV対応|Data Integrity対応プリントソフトウェア
DIに対応して、印刷物を管理します。詳細はこちら
